先端ナノ・バイオ科学専攻 Major of Advanced Nanociences and Biosciences
Creation and analysis of RNA functions and structures
 ナノサイズ機能性分子設計学 Nano-Size Functional Molecule Design Chemistry
ナノサイズ機能性分子設計学 Nano-Size Functional Molecule Design Chemistry井川 善也 Yoshiya Ikawa
- TEL : 076-445-6599
- URL : http://www3.u-toyama.ac.jp/orgsyn3/
- Keywords : ribozyme, riboswitch, RNA nanostructure, RNA design
研究の背景と目的 Background and Purpose of Study
DNAやRNAの核酸高分子は生体内での遺伝情報の保持や伝達を担う。DNAが生体内では二本鎖構造によって遺伝情報を保持するのに対し、RNAは一本鎖として生合成され遺伝情報の伝達機能を担うと共に、一部のRNAは三次元構造へと折り畳まり、触媒機能や分子認識機能など蛋白質類似の機能を立体構造に依存して発揮する。これら生体分子の高度な分子機能をナノテクノロジーに応用する研究も活発になされ、殊に2006年のDNAオリガミの報告を端著に、DNAを素材として「幾何学的な集積ナノ構造」を自在にデザインし人工機能を付与する研究は急激に発展している。さらにDNAオリガミの方法論はRNAを素材とした幾何学的ナノ構造構築へも応用されつつある。以上のようにRNAナノ構造の構築には、天然RNA構造の形成原理、幾何学的ナノ構造のデザイン原理の大きく異なる二つの原理が考えられる。 当研究室ではRNA立体構造とそれに基づく高次機能の発現に興味を持ち、リボザイムやリボスイッチなどの高度な機能を有する天然RNAについて、その構造-活性相関を解析することで、それらの生体機能の解明を行なっている。 さらに天然RNA構造の形成原理を発展させ、天然RNA構造を単位ユニットとして規則的に集積し、幾何学的なナノ構造を構築する方法論の開拓にも力を入れている。本法は上記の2つのRNA構築原理を融合し両手法の長所をしてナノ構造を創成する点が特徴である。本法の開拓を通じ、新たなRNA分子の機能構造の創成を目指して研究を進めている。
Self-assembly of nucleic acid polymers is a crucial property supporting cellular biological systems. DNA duplex structure enables storage of genetic information. RNA is synthesized as a single-strand not only to transmit genetic information but also folds into defined 3D structures to conduct biological functions such as enzymatic catalysis and molecular recognition. Self-assembly of nucleic acids is an attractive property in the field of nanotechnology. DNA has been regarded as one of the most promising materials for designing 2D and 3D nano-objects with defined sizes and shapes. With the development of DNA origami technology, a variety of artificial geometrical DNA nanostructures have been made with not only static but also dynamic structural properties. RNA has been considered as a candidate for nanotechnology material because of not only its similarity with DNA but also its functional roles (such as catalysts and receptors) in naturally occurring cellular systems. While RNA design allowed us to produce polygonal and polyhedral RNA nano-objects, this type of RNA nanostructures is distinct from naturally occurring RNA 3D structures elaborated through biological evolution. Our laboratory is interested in a broad range of RNA functions that are conducted through formation of 3D RNA nanostructures. Research on structure-function relationship of naturally occurring RNAs involving ribozymes and riboswitches is our main subject. We also highly interested in the other subject related to RNA nanotechnology, in which we are developing new design strategy to merge artificial geometrical RNA nanostructures and naturally occurring RNA 3D structures. This new strategy allows us to generate a new class of RNA nano-objects with enzyme-like functions.
本研究の領域横断性
当研究室の研究課題は、細胞内機能性RNAの解析の点では理学的かつ基礎生化学的であり、他方でRNAナノ構造を人工創成する点ではバイオ工学的である。またそれら成果の応用面では薬学、医学と連携するため、領域横断性は高い。
研究内容
自己スプライシング活性を有するモジュール集積型の大型リボザイムであるグループIリボザイムを人工集積させた「リボザイム・ナノ集積体」をデザインした。グループIリボザイムはP5部位末端において大小二つの構造モジュール(コアRzとP5モジュール)に物理的に分割でき、さらに二つのモジュールRNAは分子間で会合する(図)。分子会合した二分子型リボザイムは、元の単分子リボザイムにほぼ遜色ない酵素活性を示す。コアRzとP5モジュールの会合はGNRAループ/レセプターの相互作用を含む数種のRNA-RNA相互作用で支えられ、両モジュールの会合は選択的かつ強固な相互作用を行なう界面での分子認識に依存する。 筆者らは分割されたコアRzとP5モジュールを野生型とは異なる部位(コアRz のP8部位末端)で人工的に再連結し、両モジュール間の強い会合によりホモ多量体を形成できることを確認した。さらに連結部位を調整すれば、多量体が閉環し環状多量体が有利に生成することも示した。ホモ多量化では、環状ホモ三量体(正三角形ナノ構造)が主に生成するが、環状ホモ四量体(正方形ナノ構造)も同時に生成する(図)。この結果から、RNAの立体構造は一定の柔軟さを有することを示している。
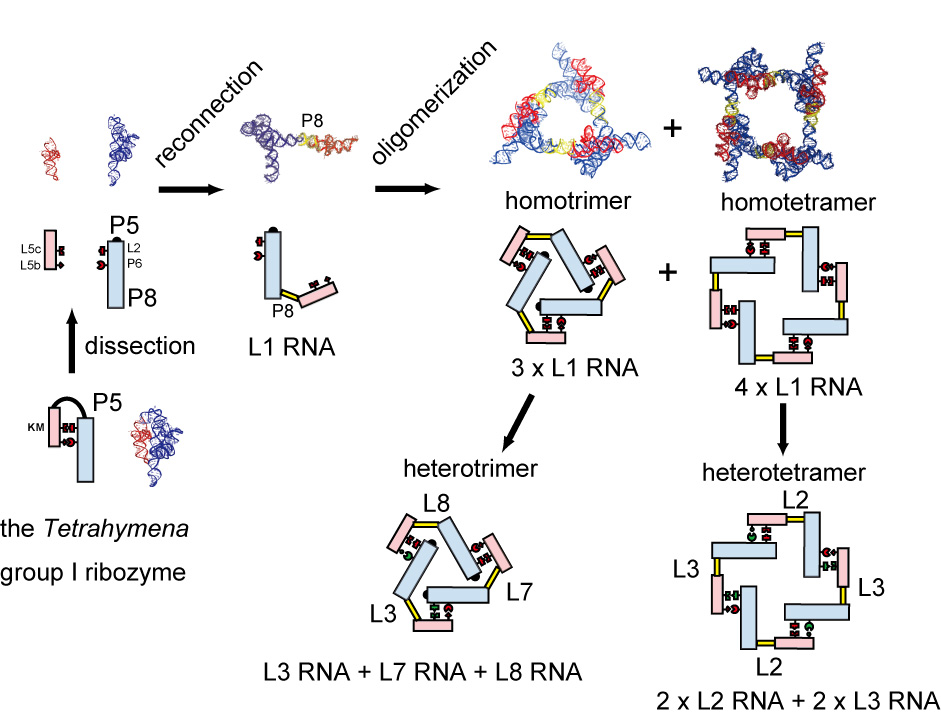
L1 RNAのホモ多量化では混在する環状三量体と環状四量体を選択的に作り分けるために、コアRzとP5モジュール間の相互作用界面の改変を試みた(図)。界面を構成する主要な2つの相互作用であるGNRAループ/レセプター相互作用と四塩基の塩基対合(それぞれ赤で表示)に対し、それぞれ第二の相互作用ペア(それぞれ緑で表示)を準備すれば、コアRzとP5モジュール間に「2×2 = 4種類」の異なる認識特異性の相互作用界面を準備できる。第二のGNRAループ/レセプター相互作用には、GGAAループを得意的に認識するレセプターを用いた。 選択的に環状4量体を生成する手法として、互いに直交性を示す2組の相互作用界面を用い2種のモノマーRNA(L2 RNA、L3RNA)を設計した。二つのモノマーRNAが共存すれば交互に集積するため、環状化の際は偶数の多角形しか生成できない(図)。2種のモノマーRNAを当量混合させると、ホモ多量化の場合とは異なりAFM観察では正方形の構造が多数観察される一方、三角形の構造は確認できなかった。環状三量体に対して3つの相互作用界面を割り振り3種のモノマーRNA(L3 RNA、L7 RNA、L8 RNA)を設計した。溶液中で会合させたところ、期待された三量体構造の高効率な生成が確認できた(図)。以上の結果から、2種および3種の相互作用界面を利用すれば、環状4量体および環状3量体をそれぞれ選択的に形成できることが示された。コアRzの複雑な立体構造さらに活用し、P5モジュールの挿入部位と相互作用界面の特異性を組み合わせれば、三角形や正方形以外の多角形、二次元シート状の集積、三次元立体構造などの多様なRNA集積も可能であろう。 さらにコアRzとP5モジュールを分子集積のユニットとして用いることで、両モジュールの会合に依存してコアRzの酵素活性の制御も可能となる。適切な条件下では、コアRz単独では活性がほぼ完全に抑制されるのに対してP5モジュールが会合すると高い触媒活性が誘導される。つまりグループIリボザイムを素材として、分子集積に連動して酵素活性が発現するナノRNA構造体を構築できる。実際に多角形構造の形成に依存して基質RNA切断活性が誘導されることも確認された。
参考文献
- Oi, H., Fujita, D., Suzuki, Y., Sugiyama, H., Endo, M., Matsumura, S., & Ikawa, Y. J. Biochem., 161, 451-462 (2017)
- Tanaka, T., Hirata, Y., Tominaga, Y., Furuta, H., Matsumura, S., & Ikawa, Y. ChemBioChem, 18, 1659-1667 (2017)
- Tanaka, T., Matsumura, S., Furuta, H., & Ikawa, Y. ChemBioChem, 17, 1448-1455 (2016)
- Tanaka, T., Furuta, H., & Ikawa, Y. J. Biosci. Bioeng., 117, 407-412 (2014)

