生体情報システム科学専攻 Major of Biological Information Systems
Joint of biosystems and electronic systems opens new bioengineering!
 生命電子工学分野 Field of Bioelectronics
生命電子工学分野 Field of Bioelectronics篠原 寛明 Hiroaki Shinohara
- TEL : 076-445-6832
- URL : http://www3.u-toyama.ac.jp/dicty/shino.html
- Keywords : Bioelectronics, Biosensor, Cell engineering, Biomolecular engineering
研究の背景と目的 Background and Purpose of Study
社会の高齢化が進み、健康で安心な生活が求められる中、健康状態を迅速、簡便にチェックすることのできるバイオセンサの開発が一層求められています。 また、数多く開発される医薬品の作用評価をいかに迅速に行うかが益々重要となり、細胞レベルでの迅速な薬物評価システムの開発が有用と期待されています。私の研究室では、製薬産業で有名な富山の地にあって、こうした社会の要望に応えるバイオセンサ・バイオセンシングシステムの開発を目的として研究を進めています。 研究の主要テーマであるバイオセンサは、微量な測定対象物質を簡単に見つけてくれる生体分子や細胞と、その分子認識反応を人の読み取り易い電気信号に変えてくれるトランスデューサとから構成されますが、私の研究室では、天然の酵素や培養動物細胞株を利用するだけでなく、蛍光性アミノ酸を部位特異的に導入した非天然変異結合タンパク質や変異抗体を合成し、人の読み取り易い信号を発する分子センサへの応用も図っています。 また、ゲート表面を測定液と接触させた際の界面電位の変化を検知するケミカル CCD や、センサ表面ごく近傍の屈折率変化をサブμmの分解能でイメージングできる2次元 SPR と言った新しいトランスデューサのバイオセンシングへの応用を世界に先駆けて研究しています。医療診断、創薬スクリーニング、食品分析などで役立つバイオセンシングの分野で世界に先駆けた研究を一緒にしませんか。
 I have studied biosensors and bioelectronics. Biosensor is a very useful tool for clinical diagnosis, home health-care, high throughput screening of drugs and food analysis etc.
We have now developed a phenylalanine sensor as a research member of Hokuriku Innovation Cluster for Health Science. Phenylalanine (Phe) is an important essential amino acid and a biomarker of phenylketonuria.
I have studied biosensors and bioelectronics. Biosensor is a very useful tool for clinical diagnosis, home health-care, high throughput screening of drugs and food analysis etc.
We have now developed a phenylalanine sensor as a research member of Hokuriku Innovation Cluster for Health Science. Phenylalanine (Phe) is an important essential amino acid and a biomarker of phenylketonuria.
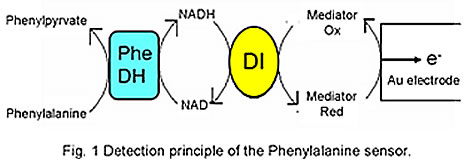
 Though blood Phe is usually detected by HPLC analysis or enzymatic analysis, these methods are still not rapid. We developed a Phe sensor chip with a disposable gold electrode on which Phe dehydrogenase (PheDH) and diaphorase (DI) were co-immobilized for Phe detection in practical use.
Chrono- amperometry with the prepared enzyme electrode chip demonstrated the increase of the catalytic oxidation current depended on the concentration of Phe. Detection range of this sensor for Phe was from 50M to 2mM. The sensor response was highly specific for phenylalanine. These results suggested that our sensor might be available to monitor Phe concentration in blood samples.
Though blood Phe is usually detected by HPLC analysis or enzymatic analysis, these methods are still not rapid. We developed a Phe sensor chip with a disposable gold electrode on which Phe dehydrogenase (PheDH) and diaphorase (DI) were co-immobilized for Phe detection in practical use.
Chrono- amperometry with the prepared enzyme electrode chip demonstrated the increase of the catalytic oxidation current depended on the concentration of Phe. Detection range of this sensor for Phe was from 50M to 2mM. The sensor response was highly specific for phenylalanine. These results suggested that our sensor might be available to monitor Phe concentration in blood samples.
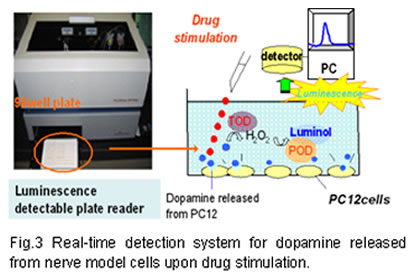 We have also studied cell-based drug sensing systems. We developed an easy, rapid and highly sensitive detection method for dopamine with the coupling of enzyme oxidation and luminol reaction. We applied this enzyme-luminescence method to observe the dopamine release from PC12 cell, a model nerve cell, upon acetylcholine or AChR agonist stimulation and succeeded in real-time monitoring of activation of the cells. Our drug detection system offered many advantages such as high sensitivity, rapid measurement and without pretreatment for cells. It may be applied to development of medicaments and various screening of harmful chemicals in foods and environment.
We have also studied cell-based drug sensing systems. We developed an easy, rapid and highly sensitive detection method for dopamine with the coupling of enzyme oxidation and luminol reaction. We applied this enzyme-luminescence method to observe the dopamine release from PC12 cell, a model nerve cell, upon acetylcholine or AChR agonist stimulation and succeeded in real-time monitoring of activation of the cells. Our drug detection system offered many advantages such as high sensitivity, rapid measurement and without pretreatment for cells. It may be applied to development of medicaments and various screening of harmful chemicals in foods and environment.
本研究の領域横断性
バイオセンサは、生体分子や細胞の機能と電子計測デバイス、電気化学デバイスや光学計測デバイスの機能とをドッキングさせて、測定対象物質を簡便、高感度に検出するシステムなので、生体分子、細胞の応答メカニズムから、計測科学の実用までを広く理解したうえで初めて設計できるため、まさに医薬理工融合の研究分野です。 バイオエレクトロニクスも正しく同様で、酵素や細胞の機能を良く知った上で、電気・電子的な制御によってその働きを計測したり、制御したりしようとする研究分野であり、これからの医工学や新しい工学のフロンティアと言えます。
研究内容
上記英文で具体的に紹介した研究内容以外にも、本研究室では以下のような培養細胞を用いたバイオセンシングの先端研究を行っています。
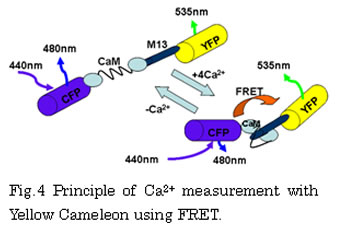
Yellow Cameleon 発現神経モデル細胞を用いた薬物バイオセンシング
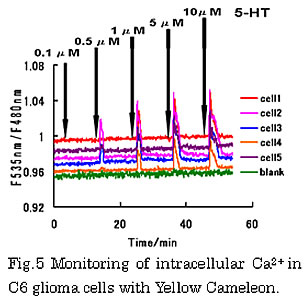
Yellow Cameleon の遺伝子を導入発現させたラットグリオーマ由来の C6 細胞をガラスベースディッシュに播き、1晩培養後、デッシュの培地を BSS に置き換えてフロー系でセロトニン(5-HT)による刺激を行った。薬物を1分間流して刺激し、(535nm/480nm)の蛍光比の変化を W-view 光学系を搭載した正立型蛍光顕微鏡システムを用いて観測したところ、図に示すように 5-HT 濃度が 0.1μM~10μM の間でその蛍光比(Ca2+ 濃度に対応)は大きく上昇し、およそ 5μM で飽和に近い状態になった。こうした結果より、Yellow Cameleon 発現神経モデル細胞を用いる薬物バイオセンシングが可能であることが示唆された。
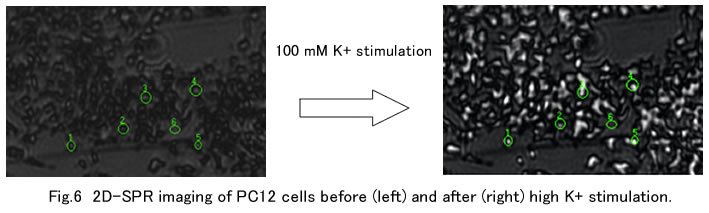
2次元表面プラズモン共鳴(SPR)イメージングによる神経系モデル細胞の興奮
応答観察
(工学系 鈴木正康教授との共同)
金薄膜を蒸着した高屈折率ガラスチップ上で神経系モデル細胞としてPC12細胞を培養した後、培地をハンクス溶液に置き換え、2D-SPR 装置のプリズム上にセットして、一定の測定角度で高K+刺激時の反射光強度の測定を行った。その結果、非細胞領域においては反射光強度がほとんど変化しないのに対して、個々の細胞領域では、30%を超える反射光強度の増加が観測された。また、細胞領域における反射光強度の増加の平均値は、K+ 濃度に依存した。この結果から、2次元SPR測定によって個々の培養細胞の興奮応答を観測でき、強いては薬物の検出に応用できる可能性が示された。 さらに、培養細胞をPKCの活性化剤である Phorbol 12-myristate 13-acetate で刺激したところ、反射光強度の増加が認められ、SPR シグナルの変化は、薬物刺激時の PKC の活性化に伴う細胞膜近傍へのトランスロケーションと関連があることが示唆された。
参考文献
- H. Shinohara, F. Wang, and S. M. Zakir Hossain, A convenient, high-throughput enzyme-luminescence detection of dopamine released from PC12 cells, Nature Protocol, 3, 1639-1644 (2008).
- S. M. Z.Hossain, H. Shinohara, and H. Kitano, Drug Assessment Based on Detection of L-Glutamate Released from C6 Glioma Cells Using an Enzyme-Luminescence Method, Analytical Chemistry, 80, 3762-3768 (2008).
- T. A. Mir, H. Shinohara and Y. Shimizu, Enzyme-luminescence method: Tool for evaluation of neuronal differentiation based on real-time monitoring of dopamine release response from PC12 cells, Analytical Methods, in press.

